Chemisorption und TPX
Die Chemisorption wird insbesondere zur Charakterisierung von Katalysatoren eingesetzt. Für Katalysatoren ist oft entscheidend, welcher Anteil der Oberfläche auch wirklich chemisch aktiv ist. Zur Bestimmung der aktiven Oberfläche verwendet man ein Gas, welches an der aktiven Komponente des Katalysators chemisorbiert, also fest gebunden wird. Oft wird z.B. Wasserstoff zur Analyse eingesetzt, der an den Edelmetallkomponenten, z.B. an Platin auf einem Platin-Alumiumoxid-Katalysator, chemisorbiert.
Physisorption vs Chemisorption
Wir bieten Chemisorptionsanalysen in vollen Umfang als Auftragsmessungen an
1. Statisch-volumetrische Methode
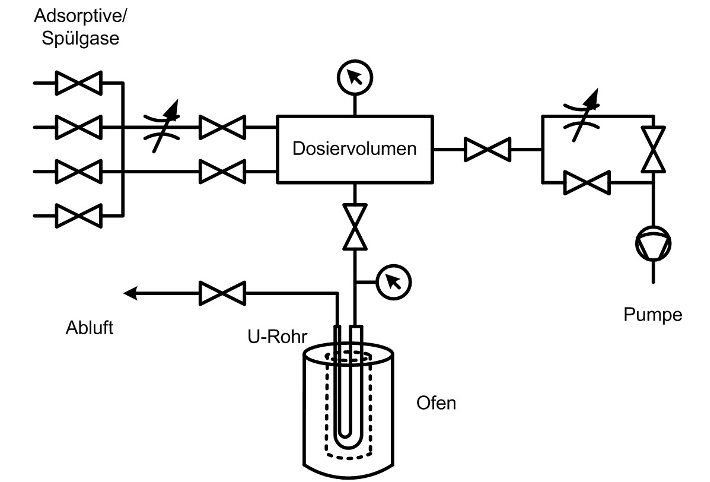
Es erfolgt die Dosierung einer bestimmten Gasmenge auf die Probe, welche sich im Vakuum befindet. Die Bestimmung der adsorbierten Mengen erfolgt durch Druckmessung innerhalb von Systemen mit bekannten Volumina. Für Chemisorptionsuntersuchungen werden oft zwei Isothermen vermessen: Die erste Isotherme ist die Summe aus Physisorption und Chemisorption. Danach wird die Probe evakuiert, um lose gebundene Gasmoleküle (physisorbiertes Messgas) wieder von der Oberfläche zu entfernen. Die Wiederholungsmessung zeigt dann nur Physisorption, da aktive Zentren nach der ersten Messung blockiert bleiben. Die Differenz zwischen beiden Isothermen ist die Chemisorptionsisotherme, aus der z.B. die aktive Oberfläche des Katalysators berechnet wird.
Versuchsaufbau Volumetrische Methode
2. Dynamische Methode
2.1. Isotherm (Puls-Chemisorption)
Ein Inertgas überströmt kontinuierlich den Feststoff. Ein Wärmeleitfähigkeitsdetektor analysiert das Messsignal (Nulllinie). Danach werden nacheinander Pulse des Messgases in den Inertgasstrom gegeben, wobei nach jedem Puls gewartet wird, bis das Messsignal auf null zurückgeht.
Anfangs nimmt die aktive Feststoffoberfläche das Messgas auf, es wird chemisorbiert. Mit der Zeit tritt Sättigung der aktiven Oberfläche ein. Die Messung wird solange durchgeführt, bis konstante Peaks am Wärmeleitfähigkeitsdetektor erscheinen, d.h. kein Messgas mehr chemisorbiert wird. Diese Methode wird auch Puls- oder Titrationsmethode genannt.
Chemisorptionsuntersuchungen werden oft auch temperaturprogrammiert durchgeführt, lesen Sie dazu mehr unter der Messmethode „Temperaturprogrammierte Reaktionen“.
2.2. Temperaturprogrammierte Reaktionen
Nichtisotherme Messungen erfolgen meist durch lineares Aufheizen einer Probe und der kontinuierlichen Erfassung der Änderung der Gaszusammensetzung. Das temperaturprogrammierte Arbeiten kann außer der Desorption (TPD), auch die Reduktion (TPR), Oxidation (TPO) oder andere, für die Katalysatorcharakterisierung relevante Reaktionen, umfassen.
Versuchsaufbau Dynamische Methode
Für die Durchführung temperaturprogrammierter Reaktionen zur Katalysatorcharakterisierung wird die Probe in-situ vorbereitet. Hierzu werden sogenannte Makros definiert, so dass die Vorbereitungsprozeduren vollautomatisch abgearbeitet werden. Die weitere Vorgehensweise ist aufgabenabhängig: Bei der TPD wird erst ein Adsorptiv auf der Probe adsorbiert (z.B. durch Puls-Chemisorption), um dann den temperaturabhängige Desorptionsprozess zu charakterisieren. Eine TPR erfolgt mit einem Reduktionsgas, meist H2, eine TPO mit einem Oxidationsgas, bevorzugt O2.
Die Messungen erfolgen im Gasstrom, wobei Änderungen der Gaszusammensetzung durch einen Wärmeleitfähigkeitsdetektor erfasst werden. Es ist also bei der Planung eines Experiments darauf zu achten, dass durch eine Reaktion nicht nur die Gaszusammensetzung, sondern auch die Wärmeleitfähigkeit des Gasstroms durch ad- oder desorbierte Moleküle verändert wird. Prinzipiell lassen sich die Gase und Dämpfe in zwei, hinsichtlich ihrer Wärmeleitfähigkeiten, deutlich unterscheidbare Gruppen einteilen:
1. H2, He
2. CO, CO2, Ar, NH3, H2O, Pyridin, N2O u.a.
Aus dieser Einteilung lassen sich die Experimente einfach herleiten, denn an einer zu untersuchenden Reaktion muss immer ein Gas/Dampf aus jeder der beiden Gruppen beteiligt sein. Beispiele:
1. TPR mit Wasserstoff (Gruppe 1) erfordert ein Trägergas aus Gruppe 2, z.B. Argon.
2. TPD von NH3 (Gruppe 2) erfordert ein Trägergas aus Gruppe 1, bevorzugt Helium.
3. TPO mit Sauerstoff (Gruppe 2) erfordert ein Trägergas aus Gruppe 1, also Helium.
Die Vorteile der temperaturprogrammierten Reaktionen bestehen in der Möglichkeit, nicht nur die aktive Oberfläche aus Chemisorptionsisothermen zu bestimmen, sondern aus der Temperaturabhängigkeit auf unterschiedlich starke, katalytisch aktive Zentren zu schließen.
 Deutsch
Deutsch English
English